
노화과정에서 활성산소의 역할
한복기 / 국립보건원 특수질환부
1. 서 론
노화의 특징인 복합성으로 인하여 다양한 현상학적인 연구결과들이 산적해 있음에도 불구하고 아직까지 노화기전은 확실하게 규정되어 있지 않다. 그런데 지난 10년간, 노화연구는 놀랄 만큼 발전하여 노화연구는
이제 초기 성년기에 접어들었다. 특히 1970년과 1980년대에 걸쳐 면역학을 비롯한 타 분야에서 개발되어 이용되었던 여러 가지 현대적 실험기법들과 분자생물학적 기법들이 오늘날 노화연구에도 적용되어 활용되고있
으며 또한 초파리와 선충류를 대상으로 한 유전학적 노화연구가 가능케 되었으며 치매나 유전적 조로증을 비롯한 노화에 따른 질환들을 연구하는 의학자들 역시 노화연구에 동참하게 되었다.
이와 같이 다양한 측면에서 이루어지는 노화연구는 크게 두 가지로 분류될 수 있다. 먼저 노화는 무작위적으로 일어난 유해한 기작들에 의한 퇴행적 변화(degenerative aging)라는 것과 또한 노화란 계획된 바대로
발생성장 단계의 마지막 종착지로서 일어난다(programmed aging)는 것이다. 이러한 논란 가운데 최근 많은 과학자들은 다시 노화의 활성산소설이라는 일련의 개념 아래로 다시 모여들고 있다. 즉, 활성산소에 의한
손상이 노화와 수명결정에 중요하다고 생각하게 된 것이다. 이 이론에 입각하여 실시된 연구들, 예를 들어 노화된 개체에서의 산화적 손상을 찾는 연구들과 분자생물학적 기법을 이용한 유전자실험에서 얻어진 결과
들도 역시 활성산소설의 신뢰도를 높이는데 기여하고 있다. 이들 결과에서 유도되는 결론은 활성산소는 퇴행적 노화현상에 관련된다는 것이며 이러한 사실은 점차 확인되어지고 있다. 따라서 노화의 생리적 유전적 혼란과 얽힘을 해결할 중요한 실마리 중 하나가 산화적 스트레스라고 말할 수 있을 것이다. 따라서 본고에서는 노화의 활성산소설과 활성산소에 관하여 자세히 살펴보고자 한다.
감사의 마음을 전하는 면역력높이기 국산 100% 항산화 프리미엄 파워킹 프로폴리스 분말 가루 플�
어버이날선물,스승의날선물, 면역력높이기, 국산100%, 프리미엄선물, 파워킹, 수용성프로폴리스, 프로폴리스분말, 프로폴리스가루, 프로폴리스, 플라보노이드,비엔케어,
smartstore.naver.com
2. 노화의 활성산소설에 대한 개요
가. 노화의 활성산소설 (the free radical theory of aging) 이란?
노화의 활성산소설은 1956년 Harman에 의해 제안되었으며, 정상적인 대사과정에서 부수적으로 생성되는 여러 가지 활성산소들에 의하여 생체구성 성분들이 산화적 손상을 받게 되고 이러한 손상들이 축적되어 노화와 죽음에 이르게 된다는 것이다. 활성산소들에 의한 손상들은 생체가 가지고 있는 방어능력으로 대처되고 있지만, 방어가 100% 완전치 못하므로 일부의 활성산소에 의한 유해작용을 받게된다. 이 유해작용은 천천히, 경우에 따라서 수년 내지는 일생을 통하여 만성적으로 일어나 누적되어 세포나 조직의 기능을 저하시키고, 이것이 곧 질병 및 노화의 원인이 된다. 그리고 이러한 유해작용이 계속될 때 마침내 죽음에 이르게 된다는 것이다. 이에 따른 현상들은 짧은 시간에는 나타나지 않으며 장시간에 걸쳐 나타나게 되는데 이것이 바로 노화과정이라고 보는 것이다.
찬물에도 잘 녹는 호주산 프리미엄 수용성 프로폴리스 분말 스틱 항산화 식품 : 부촌
프리미엄프로폴리스, 항산화식품,수용성프로폴리스,프로폴리스가루,플라보노이드,프로폴리스분말,프로폴리스추출물, 호주산프로폴리스, 호주 프로폴리스, 프로폴리스영양제,항산화도움,면역
smartstore.naver.com
나. 활성산소란 과연 무엇인가?
활성산소란 산소라디칼(oxygen free radical) 및 이것으로부터 파생된 여러가지 산소화합물들을 통칭하는것으로, 이들은 모두 반응성이 높은 특징을 가지고 있다. Free radical이란 화학적으로 최외각 전자궤도에
쌍을 이루고 있지 않는 전자를 지닌 원자나 분자를 의미한다. 이들은 이 쌍을 이루고 있지 않는 전자를 잃거나 혹은 주위로부터 전자 하나를 더 얻어 보다 안정된 상태로 가려는 성질을 가지고 있기 때문에 불안정하다. 따라서 주위의 화합물과 쉽게 반응하여 전자를 잃거나 얻으려 하기 때문에 높은 반응성을 갖는다.
그러면 산소분자(O2)가 oxygen free radical로 전환되는데 어떤 특성을 가지는지 알아보자. 그림 1에서 보는 바와 같이 산소는 원래 쌍을 이루고 있지 않는 전자를 두 개나 가지고 (이에 산소를 biradical이라고도 부른다) 있지만 다른 free radical과는 달리 반응성이 아주 낮다. 왜냐하면 산소의 쌍을 이루고 있지 않은 두 전자는 같은 spin(↑↑)을 가지고 있고, 산소에 들어갈 전자쌍은 pauli원리에 따라 상반되는 spin(↑↓)을 가지고 있기 때문이다(그림 1 참조). 그러나 산소가 이 spin restriction을 이겨내고 전자를 받아들이면, 문제의 활성산소가 생성되는 것이다. 모든 분자가 라디칼을 형성 할 수 있지만, 특히 산소 라디칼이 문제시되는 것은 호기성 생명체에서 산소의 이용은 필수불가결한 것이며 세포내 전자전달계로부터 이탈된 전자가 산소에 전달되어 산소라디칼이 생성되기 때문이다. 다음으로는 활성산소의 생성과 그 종류를 알아보자.
산소가 전자하나를 받게되면 O2-·이 되며 이를 superoxide radical(또는 superoxide anion)이라고 하며 이것은 곧 또 다른 전자 한 개와 2개의 H+과 결합하여 H2O2인 과산화수소가 된다. H2O2에 또 하나의 전자가 들어가면 산소-산소 결합이 끊어지며 수산이온(HO-)과 HO·이 생성되는데 후자를 hydroxyl radical이라고한다.
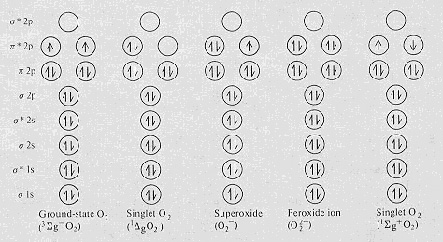
한편 전자수에 변동 없이 산소가 외부로부터 energy를 받으면 쌍을 이루고 있지 않는 전자 중 어느 하나의 spin이 변화되어, 쉽게 전자를 받을 수 있는 상태가 되어 높은 반응성을 나타내는 singlet oxygen(1O2)이 생성되는데, 이 또한 활성산소에 속한다(그림 1).
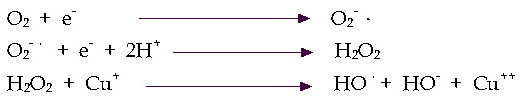
이와 같은 활성산소들이 생체내에서 생성된다는 사실은 HO·를 측정하므로서 1954년 Conmoner에 의하여 최초로 보고되었다. 또한 1969년 Fridovich에 의하여 체내에 효소 superoxide dismutase(SOD)가 발견되었는데, O2-·를 제거하는 이 효소의 발견은 체내에서 O2-·가 생성됨을 직접적으로 보여주는 확실한 증거라 하겠다.
그 후, 많은 연구들에 의하여 정상과정에서 뿐만 아니라, 염증 등의 병적상태에서도 활성산소가 생성됨이 밝혀졌으며, 또한 여러 가지 항산화 효소와 항산화인자들이 발견되어 생체내에는 복잡한 항산화체계가 발달되어 있음이 밝혀졌다. 다음으로는 활성산소의 생성과 반응 그리고 체내 항산화체계에 관하여 알아본다.
다. 활성산소의 생성
활성산소들은 체내 각종 세포들의 여러 대사과정에서 끊임없이 생성되고 있다. 그 예로서 미토콘드리아의 전자전달계, peroxisome의 지방산 대사과정, cytochrome p-450 반응 그리고 포식세포들에 의한
respiratory burst과정 등을 들 수 있다.
Mitochondria 전자전달계에서는 NADH나 succinate로부터 받은 전자가 각 전자전달복합체를 따라 단계별로 전달되어 결국 O2를 환원시켜 물로 된다. 그러나 이러한 전자전달계의 중간단계에서 전자가 이탈되어 바로 산소로 전달되면 O2-·를 형성하게 되는 것이다. 이 생성된 O2-·는 SOD 등에 의하여 H2O2가 되므로, 결국 주로 O2-·와 H2O2들이 생성된다. 그러면 Mitochondria에서는 얼마나 많은 O2-·와 H2O2가 생성되는가? In vitro에서 분리된 Mitochondria로부터 측정한 결과 전달되는 총 전자의 1∼2%가 H2O2생성에 사용되었다. 그러나 이때 사용한 buffer에는 공기가 포화되었을 것이므로 체내에서와는 달리 약 20%의 산소가 녹아있었을 것이다. 뿐만 아니라 제공된 Mitochondria의 기질농도도 실제 생리적 농도보다 높았다. 따라서 좀 더 생리적으로 유사한 조건에서의 H2O2생성은 총 전자의 0.1∼0.2% 정도가 될 것이다. 그러면 생성된 Mitochondria H2O2 중에서 O2-·로부터 만들어진 것은 얼마나 될까? Mitochondria내에 SOD가 있기 때문에
Mitochondria로부터 직접 O2-·생성을 측정할 수는 없다. 그러나 SOD가 제거된 Mitochondria 분획에서 O2-·와 H2O2 생성의 비율은 약 1.5 ∼2.1이다.
두 분자의 O2-·가 한 분자의 H2O2로 전환되므로, 모든 Mitochondria H2O2는 O2-·로부터 만들어진다고 생각된다. 그리고 세포내 H2O2의 대부분이 Mitochondria에서 생성되므로, 전자전달계에서의 O2-·생성이 세포내에서 가장 주된 산화제 생성원이라 할 수 있다.
또한 peroxisome의 지방산 대사과정에서도 활성산소가 생성된다. 그러나 peroxisome에는 고농도의 catalase가 존재하므로 peroxisome에서 생성된 H2O2가 유리되는지 또 세포질의 oxidative stress에 얼마만큼 유의성있게 기여하는지는 확실하지 않다. 그러나 일부 돌연변이성 발암물질들은 peroxisome의 숫자를 증가시키는데, 이들은 간암을 유발시키며 산화적 스트레스에 의한 손상을 증가시킨다. 뿐만 아니라, microsome의 cytochrome p-450 관련 효소들은 외인성 물질들을 대사하는 과정에서 직접 산소를 O2-·로 전환시키거나 또는 cytochrome p-450로부터 전자를 redox cycling에 관여하는 분자를 거쳐서 산소에 전달한다. 이 경우 O2-·생성과 함께 전자전달체가 동시에 재생되므로 지속적인 O2-·생성이 이루어질 수 있다. 비록 정상상태에서 cytochrome p-450에 의한 반응이 어느 정도 일어나는지는 확실치 않지만, 이러한 만성적인 p-450에 의한 O2-·생성은 갑자기 높은 농도로 toxin이 주어졌을 때 해독작용을 담당하는 능력에 영향을 줄 수 있을 것이다.
마지막으로 포식세포(phagotcytic cell)들에 의하여 활성산소가 생성된다. 이 세포들은 O2-·, ·H2O2, HClO 등의 여러 가지 산화제를 대량 생성하여 병원체나 이물질제거를 위한 방어기전으로 이용한다. 따라서 상기한 세 가지 체내 산화제 생성과는 달리 세포작용의 결과 활성산소가 생성되는 것은 아니다.
이외에도 여러 효소들에 의하여 활성산소들이 생성될 수 있으며 이는 종종 조직에 따라 다르다. 그 한 예를 들면, 일부 neuron에서 monoamine oxidase에 의하여 dopamin이 탈 아미노산될 때 H2O2가 생성되며 이는 parkinson질환의 원인이 되기도 한다.
Harman에 의하여 언급된 노화의 활성산소이론은 어느 생성원에서 활성산소가 생성되었느냐는 개의치 않는다. 그러나 생존가설(rate of living hypothesis)에서는 Mitochondria의 O2-·와 H2O2 생성에 주로 관심을 갖는다. 왜냐하면 Mitochondria의 호흡률과 수명이 반비례하기 때문이다. 또한 상기한 활성산소 생성원들 중에서 조직이나 세포의 기능에 따라 그 작용이 다를 경우 노화와 관련하여 설명할 수가 없다. 따라서 Mitochondria의 O2-·와 H2O2 생성은 수명과 관련하여 더욱 큰 주목을 받고 있다.
라. 활성산소의 반응
생성된 활성 산소는 언급 한 바와 같이 반응성이 높기 때문에 주변의 어떤 물질들과도 쉽게 반응한다. 따라서 주된 생체 구성성분인 지질 단백질 핵산들에 쉽게 활성산소들이 작용하며, 이들의 산화적 손상에 관하여는 수없이 많이 보고되고 있다.
지질의 산화는 활성산소에 의한 손상으로서 오랫동안 잘 알려져 있으며, 지방 썩는 냄새가 나는 것이 지질의 과산화 반응에 의한 것이다. 지질의 hydroperoxyl radical은 이웃한 불포화지질의 이중 결합쇄로부터 수소원자를 하나 빼앗아 hydroperoxide와 alkyl radical로 된다. 그리고 alkyl radical는 산소와 결합하면 새로이 hydroperoxyl radical로 되고 이는 연쇄적인 산화반응을 일으킬 수 있다. 이때 불포화된 알데히드를 비롯한 여러 가지 부산물들이 만들어지고 이들은 활성을 가지며 돌연변이원으로 작용하거나 효소들의 활성을 억제할 수 있고 또는 단백질이나 핵산과 작용하여 cross-link를 이루기도 한다. 더욱이 지질과산화에 의하여 세포막의 유동성이 감소되고 막단백질의 손상이 초래되기도 한다.
핵산이 산화적 손상을 받으면 8-OH-dG를 비롯한 여러 가지 DNA adduct들이 생성되고 DNA의 strand break를 일으키거나 protein 등의 다른 분자들과 cross link가 일어난다. 이러한 반응들은 유전자 돌연변이나 전자 전달과정에 영향을 미쳐 정상적인 유전자발현에 변화를 초래한다.
한편, 단백질이 산화적 손상을 받게되면 단백질 분자내의 sulfhydryl group의 산화 또는 disulfide의 환원, 아미노산 잔기의 산화적 변형, aldehyde와의 반응, 단백질간의 cross-link 그리고 peptide손상 등이 일어난다. 활성부위에 철과 같은 금속을 함유한 효소들은 O2-·에 의하여 특히 쉽게 손상된다. 또한 각 단백질들은 산화적 손상에 대한 민감도에 차이가 있는데 이는 노화현상중 하나인 항상성을 잃어버릴 가능성을 제시하는 것이다.
이상과 같은 활성산소에 의한 세포구성성분의 손상은 금속이온이나 높은산소분압에 의하여 증가될 수 있다. 예를 들어 Fe++와 Cu++와 같은 금속이온들은 Fenton반응 등을 촉매하여 많은 활성 산소가 생성될 수 있다. 또한 사람은 노화될수록 체내 철분 함량이 증가되는데 이는 나이가 많을수록 산화적 손상을 받을 위험도가 증가되는 것과 관련이 있을 수 있다.
마. 항산화 방어기전
놀랄만큼 정교하게 발달되어있는 세포내 항산화 방어체계는 크게 효소계와 비효소계로 나눌 수 있다. 이들은 항산화 효소계인 SOD, Catalase, GSHpx, 친수성 항산화인자인 ascorbate, urate, glutathione, 소수성 항산화인자 tocopherol, flavonoid, carotenoid, ubiquincol들이 있다. 그 외에 관련요소로서 비효소계 항산화인자들이 산화되었을 때 환원시키는데 필요한 효소들인 GSH reductase dehydroascorbate reductase과 protein thiol을 유지시키는 thioredoxin reductase 들이 있으며 또한 환원에 필요한 환경을 유지시키는데 관련된 효소들 예를 들면 glucose-6-phosphate dehydrogenase 등이 있다. 이러한 항산화 방어체계의 분포는 개체간에, 조직간에 심지어 세포 내 소기관들 사이에도 차이가 있다. 예를 들면 GSHpx는 포유류에서는 매우 중요한 역할을 하는 반면 파리나 선충에는 존재하지도 않는다. 또한 사람에게는 3종류의 SOD가 있는데 세포질에 있는 CuZn-SOD, Mitochondria에 있는 Mn SOD, 세포외에 존재하는 SOD들로서, 각 SOD들의 세포 내 분포가 다르다.
동물종들 사이에서 볼 수 있는 항산화제 또는 산화적 손상을 회복시키는 기작 등의 항산화방어력의 차이로서 수명의 차이를 설명할 수도 있을 것이다. 산화적 손상을 회복시키는 기작들에 관하여는 항산화요소와는 달리 많이 연구되어 있지 않았지만, 실제로 세포에서 산화된 지질, 핵산, 단백질들은 회복되며 이와 관련된 효소들도 잘 발달되어 있어 항산화 방어체계로서 간접적으로 작용한다. 이와같은 노화과정에서의 산화적 스트레스의 역할을 (그림 2)에서 도식화하여 활성산소의 생성과 항산화적 보호체계 그리고 산화적 손상의 회복기작 3가지 요소의 상호관련성을 살펴보았다.
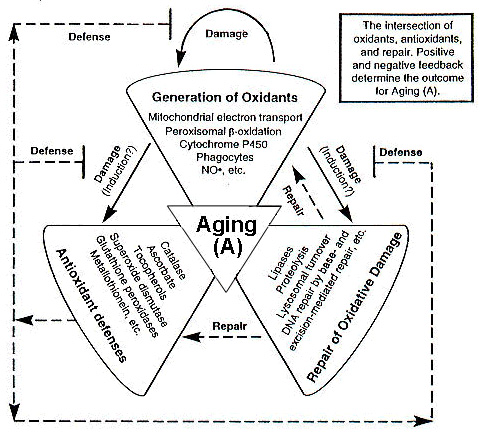
3. 노화와 활성 산소의 관련성
1956년 활성산소설이 제시된 이래 노화의 활성산소설을 뒷받침 해주는 실험적 결과는 여러 가지가 있으나, 노화에 활성산소가 관여한다는 것은 다음과 같은 사실로부터 알 수 있다. 우선 기초대사율(basal metabolic rate)과 수명은 반비례 관계에 있다. 다음으로 노화과정이 진행됨에 따라 활성산소에 의한 산화적 손상물들이 증가된다는 것이다. 마지막으로 항산화제를 처리하거나 항산화력이 높아지면, 평균 수명이 연장된다는 것이다. 이에 관하여 좀더 자세히 살펴보면, 몸집이 큰 동물이 적은 동물보다 오래살며 동물이 클수록 단위 체중당 대사율 즉, 산소소비량이 적다는 것이다. 다시 말하면 기초대사율이 높으면 높을수록 그 만큼 단위 시간당 소모되는 산소량이 많으며, 이에 따라 생성되는 활성산소량도 증가하게되어 활성산소에 의한 유해작용을 더 많이 받는다는 것이다. 더욱이 음식물 섭취를 제한하거나 운동량을 감소시키거나 또는 사육온도를 조절하여 대사율을 저하시켜 본 결과 몇가지 종류의 동물에서 평균수명이 현저히 연장되는 것이 관찰되었다. 쥐의 경우 먹고싶은 데로 먹게하여 (ad libitum) 사육한 경우 평균수명은 약 24개월인데 비해, 음식 섭취량을 60%로 줄여서 사육하면 36개월로써 거의 1.5배로 평균수명이 증가됨이 관찰되었다. 또한 곤충과 파충류와 같은 냉혈동물은 낮은 온도에서 사육하면 수명이 확실히 연장된다. 예를 들면 초파리의 경우 10。C에서의 평균수명은 120일인데 반하여 30。C에서는 14일에 지나지 않는다. 운동량 변화로 대사율을 조절하였을 때도 같은 결과가 관찰되었다. 즉 집파리의 날개를 제거하거나 조그만 병에 가두어 운동량을 제한시키면 수명이 현저히 연장되었다. 이와 같은 결과들은 대사율에 변화를 줄 수 있는 요인이 수명에 영향을 준다는 사실을 보여주는 것이다.
뿐만 아니라, 활성산소에 의한 산화적 손상의 산물들인 지방갈색소, 지질과산화물(lipid hydroperoxides),말론디알데히드(malondialdehyde), 카르보닐(carbonyl)기 및 히드록시데옥시구아노신(8-hydroxy-2'-deoxyguanosine) 등이 실험동물에서 노화에 따라 이들의 조직에서 증가된다는 것이 밝혀졌다.
이와 같이 활성산소에 의한 산화작용이 노화의 원인이라면, 항산화제와 같은 약물로서 이 산화반응을 억제시킬 경우, 수명은 연장될 것이다. 실제로 생쥐의 경우 항산화제의 하나인 mercaptoethylamine을 먹이면서 사육하였을 때 평균수명이 24개월에서 31개월로 현저히 증가되었다. 또 다른 항산화제인 santoquin을 함유한 사료 역시 생쥐의 평균수명을 18% 증가시켰다. 한편 나이가 들어 늙어감에 따라 활성산소에 대한 방어능력이 감소한다는 사실도 보고되었는데, 늙은 쥐의 간에서 분리된 SOD는 젊은 쥐의 그것보다 열에 약하고 활성도도 낮았다. SOD 이외의 방어기전인 glutathione의 농도 및 glutathione reductase의 활성 역시 늙은 쥐에서는 저하되어 있음이 관찰되었다. 또한 Cutler 등은 어느 종의 최대수명은 그 종의 항산화력에 비례한다고 주장하였는데, 특히 초파리에 항산화효소인 superoxie dismutase와 catalase의 활성을 높여 주면 수명이 30% 이상 증가한다
이와 같이 활성산소는 정상적인 대사과정 중에 생성되어, 생체 구성성분들과 반응하여 산화적 손상을 일으켜 노화와 죽음을 초래한다. 이 활성산소설에 의하면, 연령 증가에 따라 저하되는 활성산소에 대한 방어능력을 증가시켜 준다면 우리의 수명은 연장될 수 있을 것이다. 또한 노화현상 뿐만 아니라 현재 현대의학의 숙제가 되고 있는 각종 성인병, 심장질환, 발암을 비롯한 불치의 질환들이 바로 활성산소의 산화적 작용과 관련되므로, 활성산소의 작용을 조절할 수 있다면 그것이 곧 노화를 지연시키고 각종 만성 질환을 예방하는 지름길이 될 것이다. 그러나 이렇게 이상적인 예방책은 아주 평범한 사실에 입각한다. 이는 상기한 여러 가지 실험결과에서 시사하듯이, 적당한 운동, 과식하지 않는 식생활 습관 그리고 신선한 야채의 섭취를 통하여 야채에 다량 함유된 항산화인자(각종 비타민C, E, 및 carotene) 를 공급받는 것이다. 이것은 곧 산화적 손상에 의한 노화과정을 지연시키거나 조절할 수 있는 가능성을 제시하는 것이라 하겠다.
참고문헌
1. Beckman, KB and Ames BN : The Free radical Theory of aging matures. Physiol, Rev. 78 : 547-571. 1998
2. Fridovich I : The biology of oxygen radicals. Science 201 : 875-880. 1978
3. Halliwell B and Gutteridge JMC : Free Radicals in Biology and Medicine. 1992, Clarendon Press Oxford.
4. Harman D : A theory based on free radical and radiation chemistry. J Gerontol. 11 : 298-3003. 1956
5. Medvedev ZA : An attempt at a rational classification of theories of aging. Biol Rev. 65 : 375-398. 1990
6. Orr, WC and Sohal RS : Extension of life-span by overexpression of superoxide dismutase and catalase in Drosophila melanogaster. Science 263(5150): 1128-1130. 1994
7. Sohal, RS, Agarwal, S and Orr, WC : Simultaneous overexpression of copper and zinc-containg superoxide dismutase and catalase retards age-related oxidative damage and increases metabolic
potential in drosophila melanogaster. J Biol. Chem. 270(26): 15671-15674. 1995
'실버산업 50+세대 > 건강' 카테고리의 다른 글
| 충격! 식약처에서 회수 및 판매중지시킨 크릴오일 12개는? (0) | 2020.06.11 |
|---|---|
| 돈되는 건강정보 치질 증상 및 자가치료법 (0) | 2020.05.25 |
| 돈되는 건강정보 비타민B12 효능 부작용 (0) | 2020.05.01 |
| 돈되는 건강정보 체리 효능 부작용 (0) | 2020.04.30 |
| 돈되는 건강정보 비타민C 효능 부작용 (0) | 2020.04.29 |




댓글